
近日,美国FDA发布了最新的《医疗器械制造商检查合规计划手册》(CP7382.850),全面更新了对医疗器械生产企业的监管框架。新规将于2026年2月2日正式生效,旨在确保医疗器械全生命周期的安全性与有效性。下述核心要点,值得所有从业者重点关注:
一、新规核心监管要求
🔍 核心转变:基于风险的检查
FDA将采用全新的“基于风险”策略安排检查优先级。高风险产品(如植入式、生命支持类器械等)、存在不良合规记录(高召回率、MDR报告频发)的企业以及首次受检的三类器械制造商,将成为重点对象。
📋 两大检查模型,针对性更强
手册明确划分两类标准化检查流程:“模型1”适用于常规或后续检查,需全面评估质量体系各领域;“模型2”适用于首次或上市前检查,聚焦核心特定要素。实现检查流程精准匹配、高效落地。
🔄 质量体系与国际接轨
FDA正式将国际标准 ISO 13485:2016 纳入质量管理体系法规(QMSR),重点强调企业质量文化建设与流程整合要求,明确企业需从设计开发、生产制造到售后服务全流程,均需严格符合风险管理要求。
⚡ 聚焦高风险与特殊环节
上市前批准(PMA):三类高风险器械需通过严苛审批流程,检查重点聚焦工艺验证与设计开发全流程合规性。
上市后监督:FDA将对已获批的高风险器械开展定期检查,同步重点关注网络安全、辐射安全等新兴风险领域。
特殊主体:二手器械再制造商、一次性器械再处理商等主体被视同制造商,正式纳入统一监管范围。
📈 监管后手:从警告到司法行动
FDA按违规严重程度明确梯度化处置措施,涵盖警告信、产品扣押、禁令直至刑事起诉等;对屡教不改的企业,将要求其聘请外部审计机构核查,并提交年度合规认证报告。
二、 企业应对新规的行动指南:六大举措即刻落地
🛠️面对已经生效的新规,医疗器械企业需快速启动合规整改工作,从体系梳理到实操落地全方位推进,具体行动举措如下:
开展差距分析
系统对比现有质量体系与QMSR新规以及ISO 13485:2016标准的所有要求,找出差距。已经获得ISO 13485:2016认证的企业会相对轻松,但仍需关注FDA的特定要求。
升级质量管理体系文件
依据差距分析结果,更新质量手册、程序文件等核心文件,确保反映新规的所有变化,特别是术语和风险管理要求的更新。
强化风险管理
确保风险管理活动覆盖产品全生命周期,从设计开发、生产到上市后监督,并符合ISO 14971标准。
准备关键文件
梳理并确保设计历史文件(DHF)、器械主记录(DMR)、器械历史记录(DHR) 以及CAPA(纠正与预防措施) 记录的完整性、准确性与可追溯性。
内部培训与沟通
针对全体员工开展新规专项培训,重点强化高层管理者、质量相关岗位人员的合规认知,确保全员理解并落地基于风险的管理思维与新流程要求。
模拟检查与自查
可以参照FDA新的检查程序手册进行内部模拟审计,熟悉可能的新检查流程和提问方式,提前发现潜在问题。
三、一图看懂:检查内容架构
无论是模式1还是模式2,检查内容都围绕以下6+4结构展开:
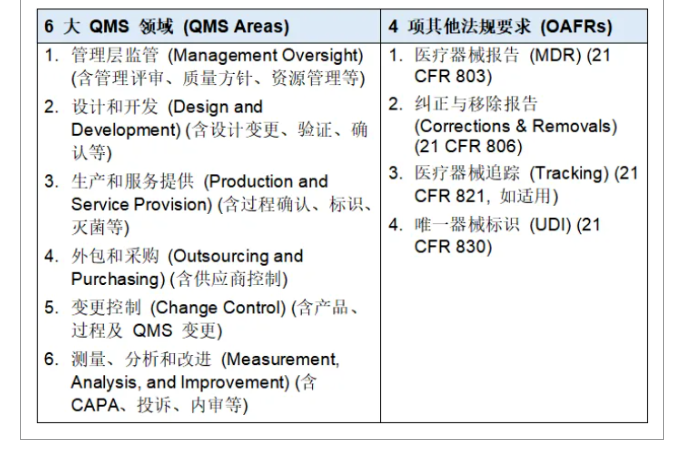
本手册正式取代了旧版文件,标志着FDA对医疗器械的监管迈入更系统、更严格、更国际化的全新阶段。相关企业应尽早熟悉新规,完善自身质量体系,以应对即将到来的检查挑战。
为助力企业精准拆解新规要点、高效落地合规整改动作,金飞鹰药械咨询技术服务集团特推出FDA新规解读与合规实操专项培训,培训时间定于2月26日下午3点,感兴趣的朋友记得锁定本次的精华课程,精准把握合规方向、筑牢体系建设根基!
信息来源:FDA 排版整理:金飞鹰药械



