三类医疗器械首次注册
- 立即咨询
-
全国服务热线:
400-888-7587

♛ 办理条件 / Conditions
申请人应为境内依法进行登记的企业
政府官方原文链接:
http://samr.cfda.gov.cn/WS01/CL1768/152060.html
۞ 申请材料清单 / List of application materials
1.申请表
2.证明性文件
3.医疗器械安全有效基本要求清单
4.综述资料
(1)概述
(2)产品描述
(3)型号规格
(4)包装说明
(5)适用范围和禁忌症
(6)参考的同类产品或前代产品的情况(如有)
(7)其他需说明的内容
5.研究资料
(1)产品性能研究
(2)生物相容性评价研究
(3)生物安全性研究
(4)灭菌和消毒工艺研究
(5)有效期和包装研究
(6)动物研究
(7)软件研究
(8)其他
6.生产制造信息
(1)无源产品/有源产品生产过程信息描述
(2)所生产场地
7.临床评价资料
8.产品风险分析资料
9.产品技术要求
10.产品注册检验报告
(1)注册检验报告
(2)预评价意见
11.说明书和标签样稿
(1)说明书
(2)最小销售单元的标签样稿
12.符合性声明
㉿ 办理流程 / Processing process
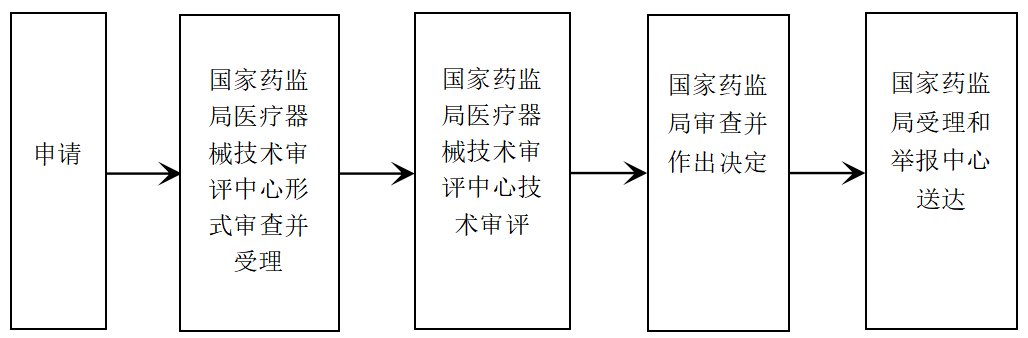
❈ 广东政务局服务承诺时间 / Service Commitment Time of Guangdong Government Bureau
名称 | 说明 | 时限 |
受理 | 5(工作日) | |
行政许可决定 | 20个工作日(不含技术审评和申请人补充资料及补充资料审评所需的时间)。20个工作日内不能做出决定的,经局领导批准,可延长10个工作日。 | 20(工作日) |
✪ 办理依据 / Processing basis
《医疗器械监督管理条例》(国务院令第650号)第十一条:申请第三类医疗器械产品注册,注册申请人应当向国务院食品药品监督管理部门提交注册申请资料。 |
〠 金飞鹰相关服务 / Golden Eagle related services
●产品分类确认或申报 ●注册单元确认 ●创新医疗器械申报 ●产品技术要求确认 ●产品样品送检文件准备 ●产品送检及检验报告跟踪 ●生产厂房规划及平面图设计 ●产品研发过程辅导 ●生产设备及检验设备、设施清单确定 ●无菌或无尘厂房设施验证 ●灭菌工艺验证 | ●包装工艺验证 ●特殊过程验证 ●注册资料申报 ●注册资料递交 ●人员培训 ●体系考核申报资料准备 ●何等考核申报资料递交 ●质量管理体系文件编制 ●产品技术文档建立 ●体系考核现场检查预检查 ●体系考核后不符合项改善 | ●注册资料发补 ●临床试验CRO ●临床试验备案 ●注册人制度质量协议 ●委托方资格申核 ●委托方委托合同 ●企业委托设计 ●产品注册专家答辩资料准备 ●产品注册专家答辩模拟 ●与政府主管机构联络及技术咨询 |
〠 结果样本 / Results the sample
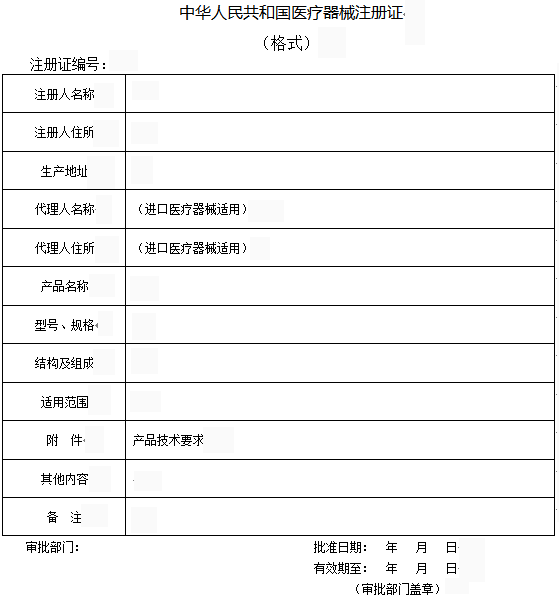
全面解决您的研发、生产、验收、营销全流程问题

practical experience
2000多个二、三类医械项目经验沉淀,为你分配做过相同案例的实战老师。
Professional translation
汇聚7大语种专业翻译精英,多年医械行业翻译经验,能准确翻译专业名词及用语。
Software development
强大的软件研发团队,已为集团研发出成熟的项目管理软件,可提供软件定制服务。
Group supply chain
严选数十个优秀的医械行业服务机构,可为客户推荐更实惠的医械配套服务。
多次创造二三类高风险产品一次性通过的行业纪录
项目状态:已结案
项目辅导老师:李老师
项目状态:已结案
项目辅导老师:车老师
项目状态:已结案
项目辅导老师:王老师
项目状态:已结案
项目辅导老师:黄老师