近日,安徽省药监局发布通告称,自2024年1月1日起,对安徽省第二类有源医疗器械首次注册项目实行立卷审查工作,有关事项具体如下:
一、立卷审查适用于第二类有源医疗器械首次注册申请事项。
二、安徽省药品审评查验中心在受理环节按照立卷审查要求,审查相应申请的申报资料,并对申报资料的完整性、合规性、一致性进行判断。立卷审查不对产品安全性、有效性评价的合理性、充分性进行分析,不对产品风险受益比进行判定。
三、申请人在准备注册申报资料时,可依据《安徽省第二类有源医疗器械首次注册立卷审查要求(试行)》进行自查,申报时不需要提交自查表。
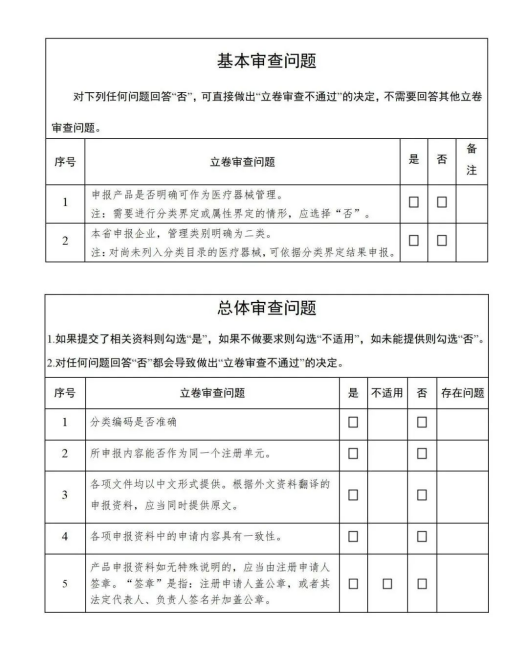
↑ 安徽省药监局立卷审查基本审查问题&总体审查问题
以上仅对通告正文内容进行转载,如需查看《安徽省第二类有源医疗器械首次注册立卷审查要求(试行)》全文,可添加文末小编微信或点击“阅读原文”。
信息来源:安徽省药监局
排版整理:金飞鹰药械
医疗器械注册咨询认准金飞鹰 深圳:0755-86194173 广州:020 - 82177679 湖南:0731-22881823 四川:028 - 68214295


